
طبقه بندی تومورهای مغزی به کمک یادگیری عمیق و یادگیری ماشین
تیمی از محققان دانشکده پزشکی واشینگتون مدل یادگیری عمیقی برای طبقه بندی تومورهای مغزی طراحی کردهاند. این مدل میتواند تومور مغزی را تشخیص دهد و در یکی از شش دسته رایج طبقه بندی کند؛ این مدل تنها از یک تصویر MRI سهبُعدی استفاده میکند. نتایج این پژوهش در ژورنال «رادیولوژی و هوش مصنوعی Radiology: Artificial Intelligence» به چاپ رسیده است.
ساتراجیت چاکرابارتی، آریستیدیس سوتیراس و دنیل مارکوس در آزمایشگاه تصویربرداری محاسباتی مؤسسه رادیولوژی مالینکرات فعالیت دارند. چارابارتی درباره این پروژه توضیح میدهد: «این اولین پژوهشی است که تومورهای درونجمجمهای شایع را موردمطالعه قرار میکند و بر اساس یک تصویر MRI سهبُعدی، حضور یا عدم حضور تومور و در صورت وجود، کلاس آن را مشخص میکند.»

شش مورد از شایعترین تومورهای درونجمجمهای عبارتاند از: گلیوما درجه بالا، گلیوما درجه پایین، متاستاز مغزی، مننژیوم، آدنوم هیپوفیز و نوروم آکوستیک. هر یک از این تومورها از طریق هیستوگرافی مستندسازی شدهاند، فرایندی که شامل نمونهبرداری از محل مشکوک به سرطان (از طریق جراحی) و سپس بررسی آن زیر میکروسکوپ است.
به گفته چاکرابارتی، رویکردهای یادگیری ماشین و یادگیری عمیق که از دادههای MRI استفاده میکنند، ظرفیت این را دارند که فرایند تشخیص و طبقه بندی تومورهای مغزی را خودکار سازند.
وی ادامه میدهد: «MRI غیرتهاجمی را میتوان به عنوان بخشی از فرایند معاینه هیستوگرافیک یا در بعضی موارد، جایگزین آن در نظر گرفت.»
چاکرابارتی و همکارانش، در مؤسسه رادیولوژی مالینکرات، برای ساخت و آموزش مدل یادگیری ماشین خود، دیتاست بزرگی از تصاویر MRI سهبُعدی از چهار منبع متنباز جمعآوری کردند: قطعهبندی تصاویر تومورهای مغزی، اطلس ژنوم سرطانی گلیوبلاستوما مولتیفرم و اطلس ژنوم سرطانی گلیوما درجه پایین. علاوه بر اینها، تصاویر MRI قبل از جراحی و همچنین اسکنهای بعد از جداسازی با T1 نیز در این دیتاست قرار گرفتند.
در مجموع 2,105 اسکن جمعآوری شدند و به سه زیرمجموعه تقسیم شدند: 1,396 مورد برای آموزش، 361 مورد برای آزمایش داخلی و 348 مورد برای آزمایش بیرونی. شبکه با آموزش روی مجموعه اول توانست بین اسکنهای گرفتهشده از مغز سالم و تصاویر حاوی تومور تمیز قائل شود و علاوه بر این، تومورها را بر اساس نوعشان دستهبندی کند. تصاویر موجود در مجموعههای آزمایش داخلی و بیرونی برای ارزیابی عملکرد مدل استفاده شدند.
مدل با دستهبندی تصاویر دیتاست آزمایشی داخلی به یکی از هفت کلاس موجود (یک کلاس سالم و شش کلاس تومور مغزی) به دقت 35/93% درصد دست یافت، بدین معنی که 336 مورد از 361 تصویر را به درستی دستهبندی کرد. میزان حساسیت مدل از 91 درصد تا 100 درصد، مقدار پیشبینی مثبت یا مثبت صحیح (احتمال تشخیص افرادی که واقعاً تومور دارند) بین 85 تا 100 درصد و مقدار پیشبینی منفی یا منفی صحیح (احتمال عدم تشخیص افراد سالم) نیز بین 98 تا 100 درصد متغیر بود.
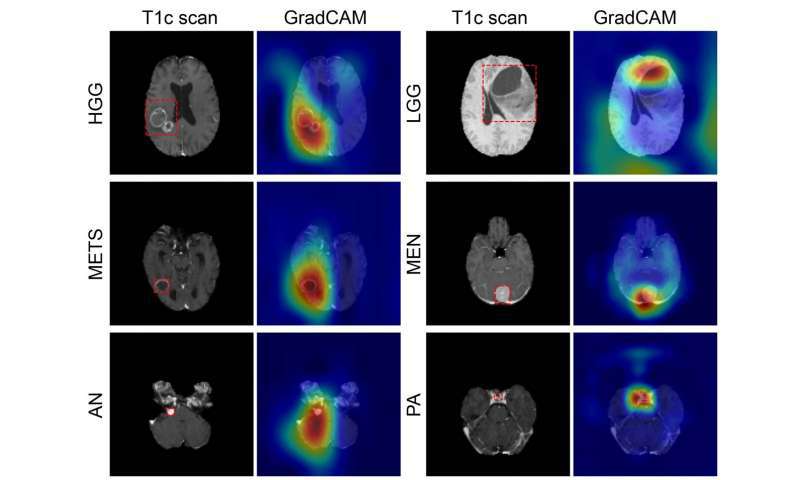
دقت مدل روی دیتاست آزمایشی بیرونی که تنها دو نوع تومور (گلیوما درجهپایین و گلیوما درجهبالا) را نشان میداد، برابر با 95/91 درصد بود.
چاکرابارتی میگوید: «نتیجه آزمایشها نشان دادند که یادگیری عمیق، پتانسیل امیدوارکنندهای در ارزیابی و طبقه بندی تومورهای مغزی به صورت خودکار، دارد. مدل ما بر روی دیتاستی ناهمگون توانست به دقت بالایی دست یابد و علاوه بر این، تعمیمپذیری فوقالعادهای بر روی دادههای آزمایشی کاملاً جدید از خود نشان داد.»
«این مدل یادگیری عمیق با بسط و ارتقای رویکردهای دوبُعدی موجود، مسیر دستیابی به گردشکاری خودکار و یکپارچه را هموارتر میکند. برای استفاده از رویکردهای دوبُعدی، رادیولوژیستها باید در ابتدا به صورت دستی مناطق مبتلا به تومور را در تصاویر MRI مشخص کنند. شبکه عصبی پیچشی میتواند فرایند پردردسر قطعهبندی تومورها را از گردشکار حذف کند.»
دکتر سوتیراس، یکی از توسعهدهندگان این مدل، معتقد است: «میتوان کارکرد این مدل را بسط داد و بر روی سایر تومورهای مغزی یا حتی اختلالات عصبشناختی نیز از آن استفاده کرد. در این صورت، گردشکارهای رادیولوژی عصبی آسانتر و سرراستتر میشوند.»
چاکارابارتی اضافه میکند: «این شبکه اولین گام در مسیر توسعه رادیولوژی مجهز به هوش مصنوعی است؛ گردشکار جدید قادر خواهد بود با تکیه بر آمار و اطلاعات کمی، تصاویر را تفسیر کند.»
جدیدترین اخبار هوش مصنوعی ایران و جهان را با هوشیو دنبال کنید





